上周,美国 “MoCRA Cosmetic Direct” 的公测版已经上线,之前用于药品注册登记的提交系统(FDA Direct)更新为“FDA Direct. CDER Direct & Cosmetics Direct”。
据悉,该版本将作为美国食品药品监督管理局 (FDA) 用于收集企业工厂注册和产品列名信息正式平台上线前的beta测试版,最后再进行系统相关功能的修正。
由于FDA已经将化妆品工厂注册和产品列名的截止期推迟到了2024年7月,企业有较充足的时间进行准备,因此需要进行工厂注册和产品列名的企业也可以等待FDA正式官宣Cosmetic Direct平台上线。
以下是瑞欧科技对公测版系统现有信息和界面的介绍:
公测版系统介绍
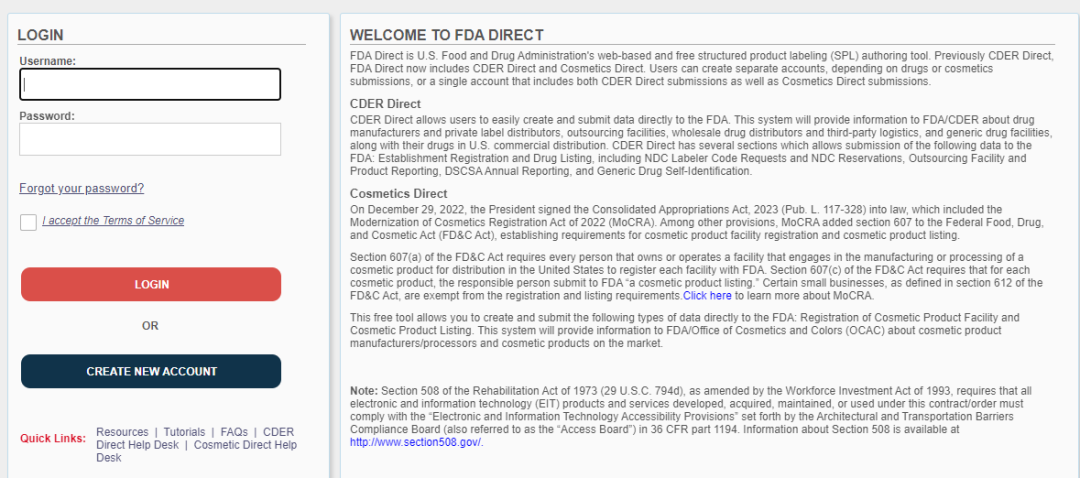
提交系统可以提供3类账户的创建:药品账户(CDER Direct)、化妆品账户(Cosmetics Direct)或者混合账户(Combined (CDER Direct and Cosmetics Direct);其中,化妆品账户的申请不需要提供邓白氏编码。
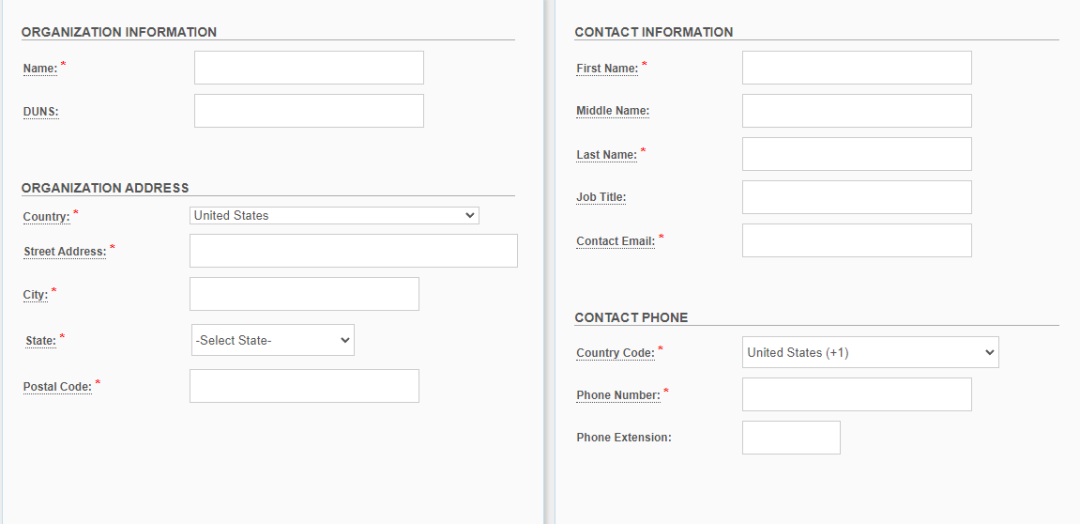
化妆品账户所需信息界面
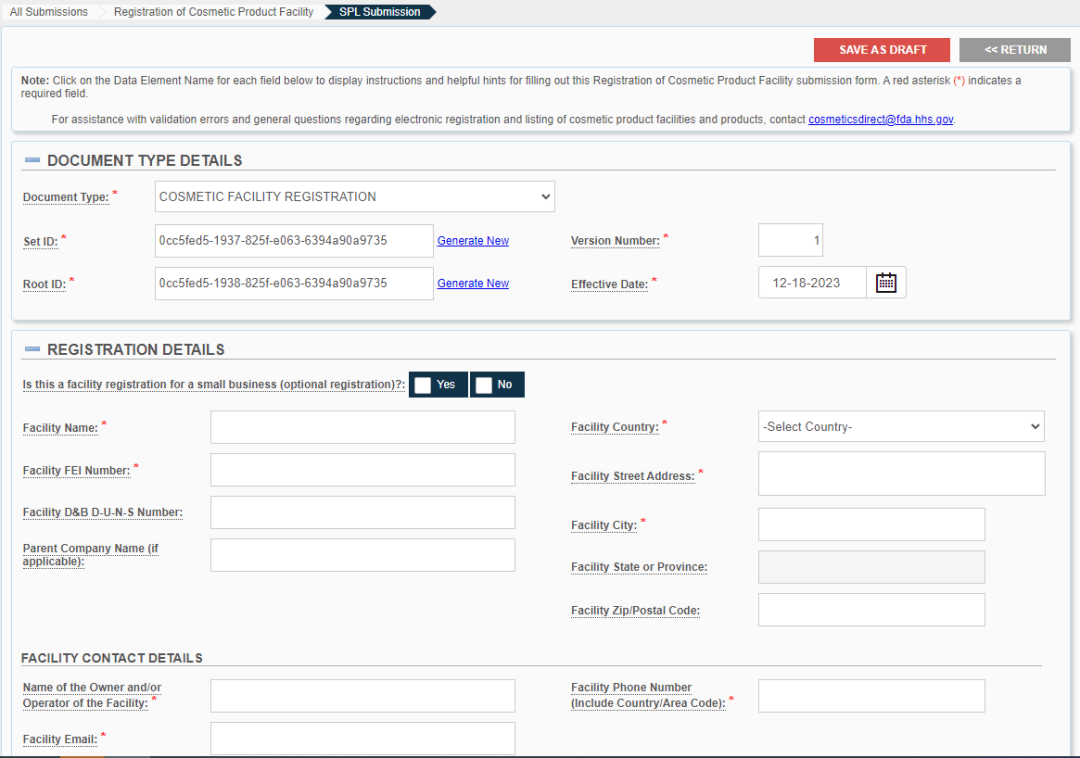
化妆品工厂注册需要提供工厂所有者的信息、FEI编号、相关的产品类别和责任人信息,等等;
化妆品产品列名需要提供相关的产品信息(责任人、成分清单等)、工厂注册号、责任人信息,等等。
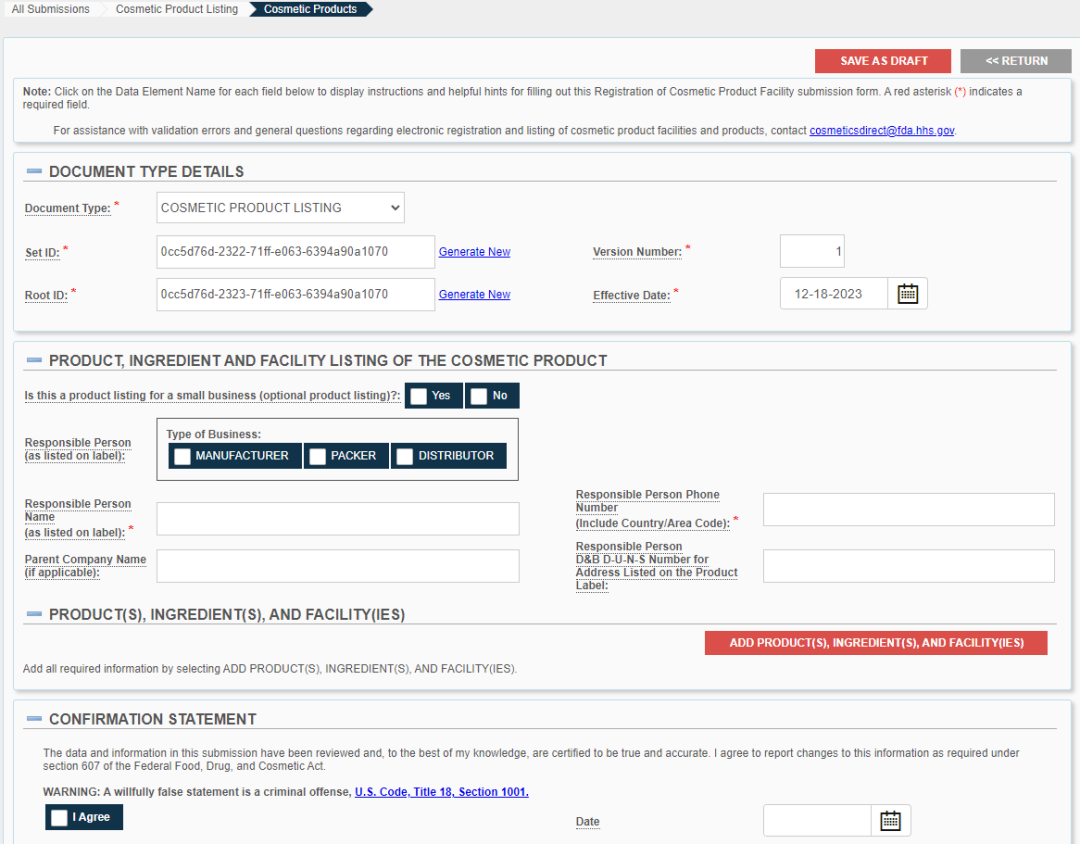
化妆品产品列名界面
系统填报说明
根据2022年12月29日颁布的MoCRA法规(《2022年化妆品法规现代化法案》),化妆品相关的生产工厂和责任人需要在规定的时间内进行工厂注册和产品列名。
2023年9月15日,FDA发布了化妆品电子提交系统指南草案。草案中对于电子提交系统的操作步骤做了详尽的说明;此次开放的电子提交系统具体操作可以参考指南草案中的相关内容。

除了电子提交系统以外,FDA还接受纸质版的工厂注册(FDA Form 5066-darft)和产品列名提交(FDA Form 5067-darft)。
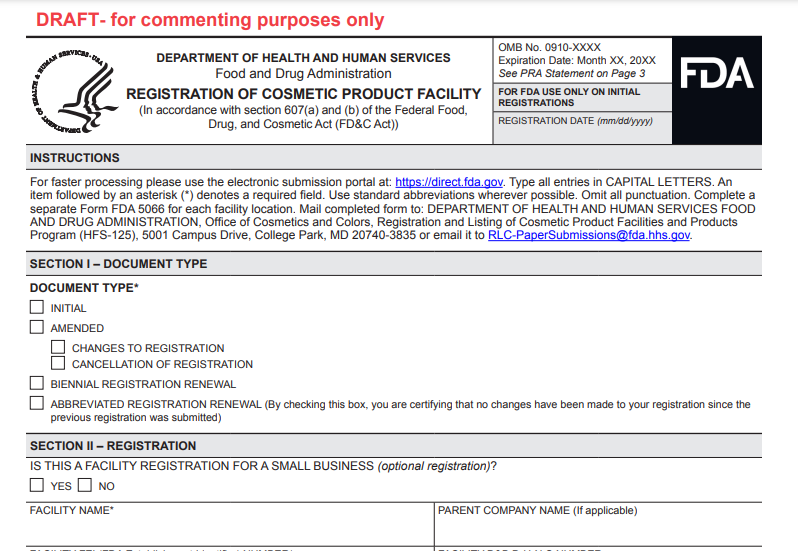

通过对比公测版与Form 5066和Form 5067的信息可以发现,系统公测版的所需信息与Form 5066和Form 5067的要求基本一致。
企业合规建议
瑞欧科技建议,相关企业可以根据MoCRA以及FDA相关指南的要求积极准备工厂注册和产品列名的相关信息和资料,并关注系统的正式上线。
具体提交信息、豁免情况以及合规建议可以参考瑞欧科技推出的 「美国化妆品法规现代化法案——工厂注册和产品列名重点解读」的线上研讨会。
相关阅读:
美国FDA更新化妆品严重不良反应报告填报说明,规范产品责任人职责!
2023全球化妆品法规动态:美国化妆品注册推迟,多国调整管理要求(11月)
美国FDA宣布推迟化妆品工厂注册和产品列名,额外给予企业缓冲期准备!
▼▼
关注“妆研24小时”
获取更多全球化妆品合规新资讯







 化学品合规
化学品合规
 化妆品合规
化妆品合规
 检验检测
检验检测
 安全管理智能化
安全管理智能化
 绿色低碳可持续
绿色低碳可持续
 药品合规
药品合规
 食品合规
食品合规
 食品接触材料/再生塑料
食品接触材料/再生塑料
 中国农药登记
中国农药登记
 境外农药登记
境外农药登记