继美国食品药品监督管理局(FDA)在今年8月7日发布了工厂注册和产品列名的指南文件征求意见稿后。
9月18日,FDA对后续工厂注册和产品列名系统拟收集的信息开启意见征求,包括系统界面的公开,以及两类纸质提交表格的草稿发布(FDA 5066表格和FDA 5067表格)。意见征集截至2023年10月18日。
瑞欧科技对发布的几份文件进行了阅读,对其中的关键信息整理如下:
注册账号页面和主页信息展示
平台名称定为Cosmetics Direct,与FDA药品提交平台CDER Direct的名称类似。
界面展示
包括工厂注册和产品列名的不同入口、相关的FDA外链和账号管理界面。

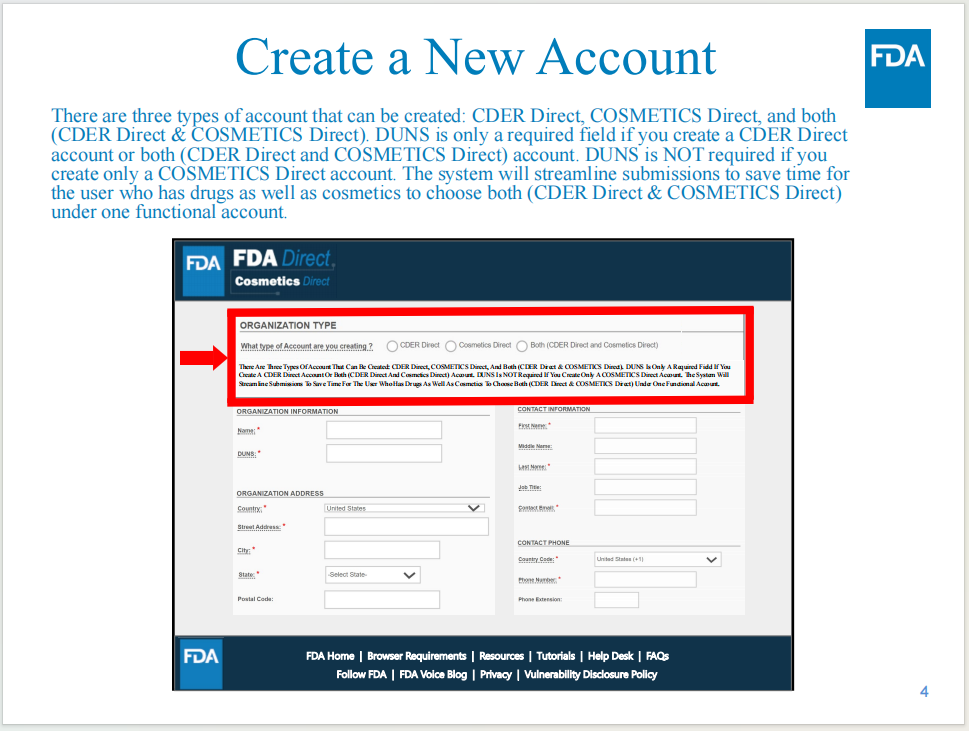
账号创建
支持同时创建Cosmetics Direct和CDER Direct两个账号,但如果仅需要创建Cosmetics Direct账号,无需提供邓白氏码。
账号创建所需信息包括:机构名称、邓白氏码(部分情况需要)、机构地址信息、联系人信息。
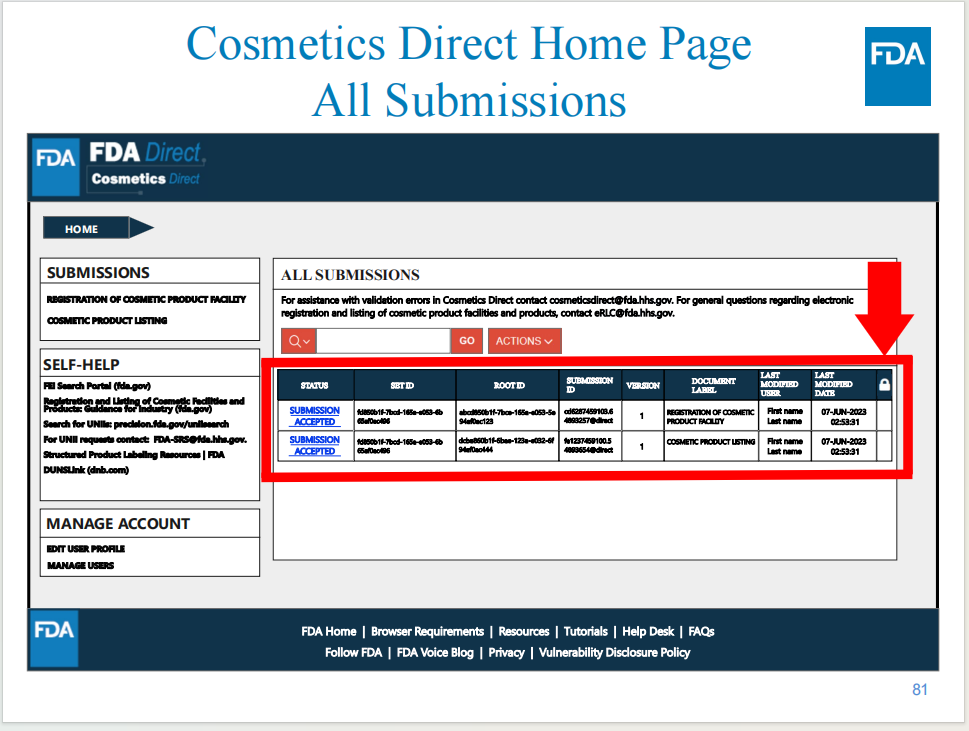
产品信息展示
所有完成列名的产品信息都可以在主页显示。
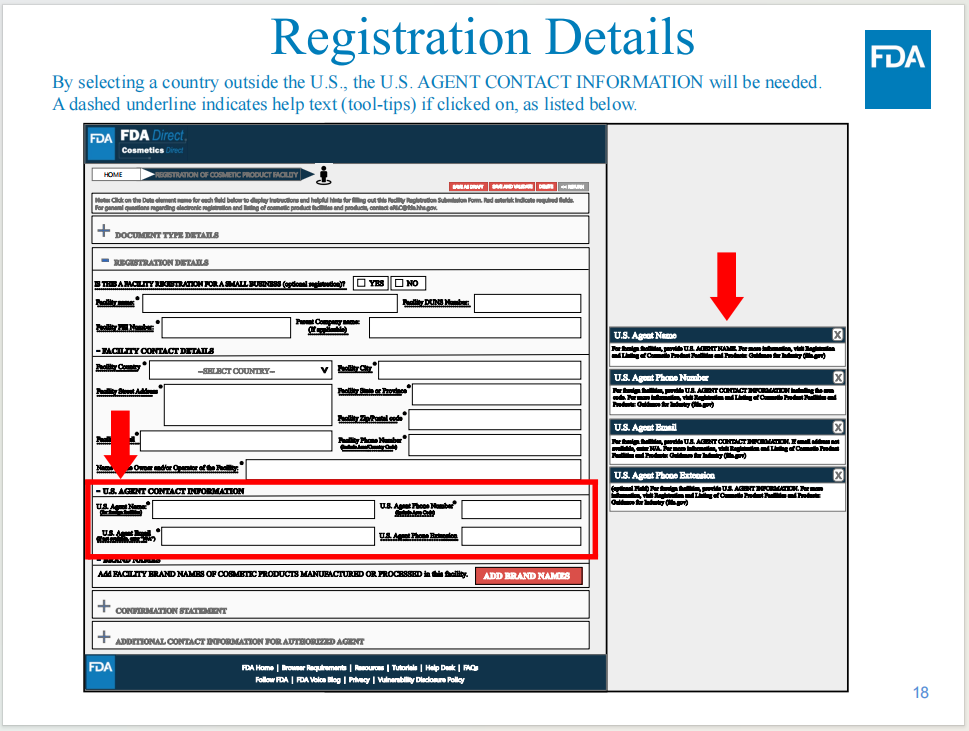
工厂注册操作界面
工厂注册操作方式,包括在平台上创建电子表格和上传SPL文件两种方式。
需要填写美国代理的公司信息和联系方式
产品信息是否为必填项尚不确定
从目前显示的界面截图来看,还无法确定进行工厂注册操作环节时相关产品品牌信息上传是否为必填项,还有待正式系统上线后验证。
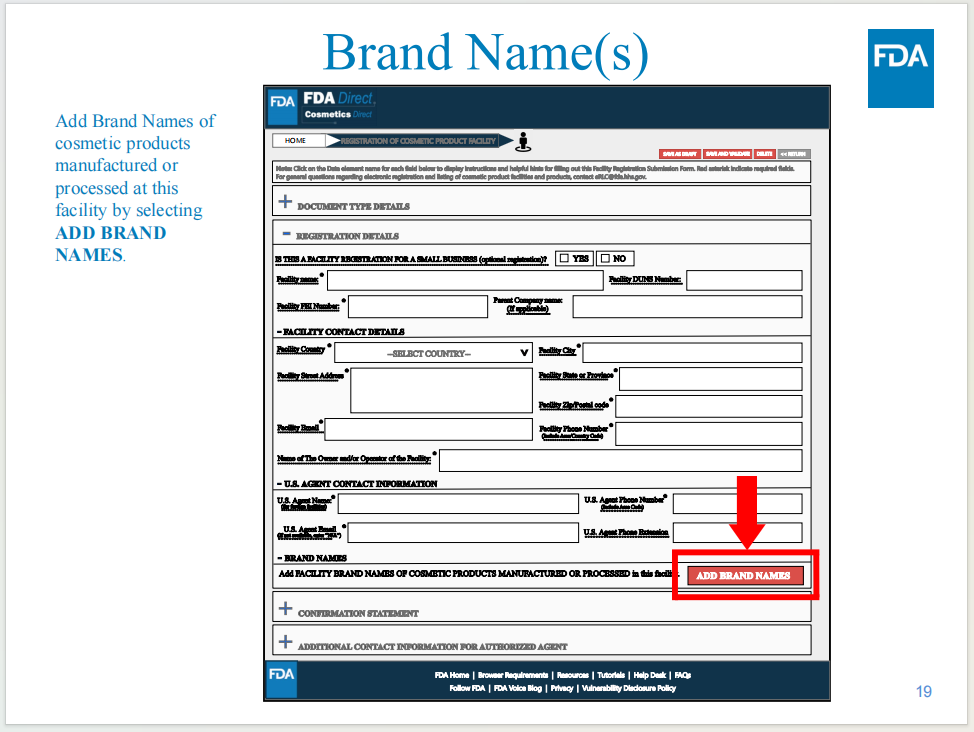
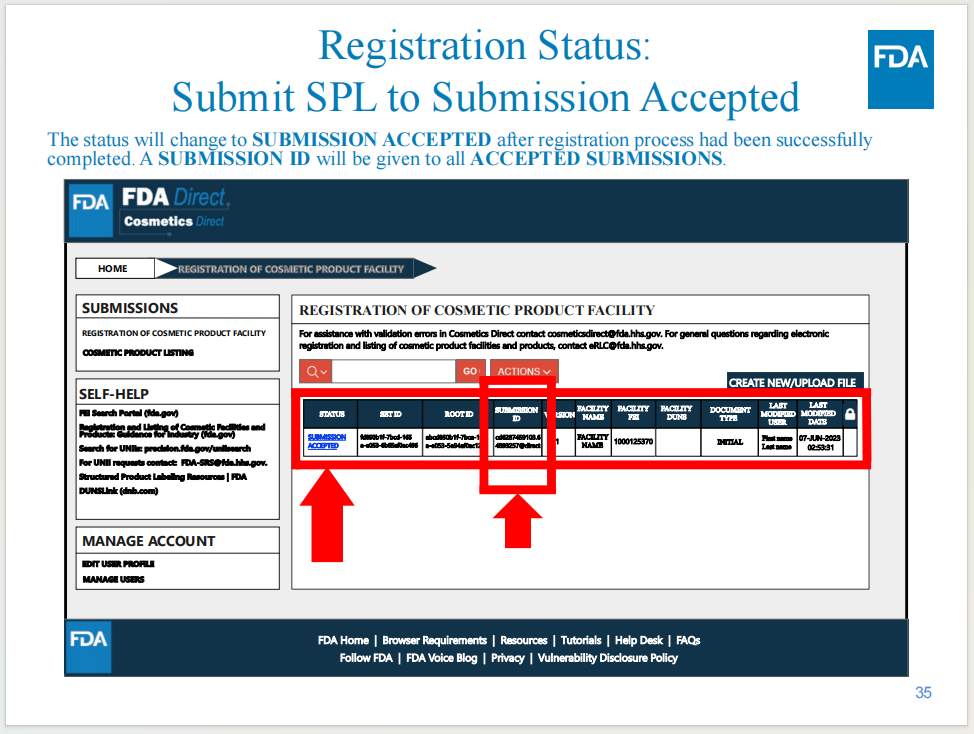
当完成递交后,会获得工厂注册号码
产品列名界面
产品操作方式,包括在平台上创建电子表格和上传SPL文件两种方式。
主要信息填写
主要需要填写的信息包括:代理人信息、产品信息、原料信息和工厂信息。

原料信息填写
原料信息上传可以通过文件上传的方式进行,但未说明接受的文件格式。
需要填写的信息包括原料的名称(需要按照美国的原料命名规则)以及UNII编号,如我们之前所推测的,并不需要填写配方的原料使用浓度信息。
*根据Fair Packaging and Labeling Act,美国的化妆品包装和标签上的化妆品成分命名需要参考 21CFR701.30 中的要求。详细的解释说明,见《超全分享 | 什么是INCI名称?如何申请INCI名称?INCI的命名规则?》。

工厂信息填写
工厂的信息中,对于非小规模企业,FEI码是必填信息。

当完成递交后,会获得产品列名号码
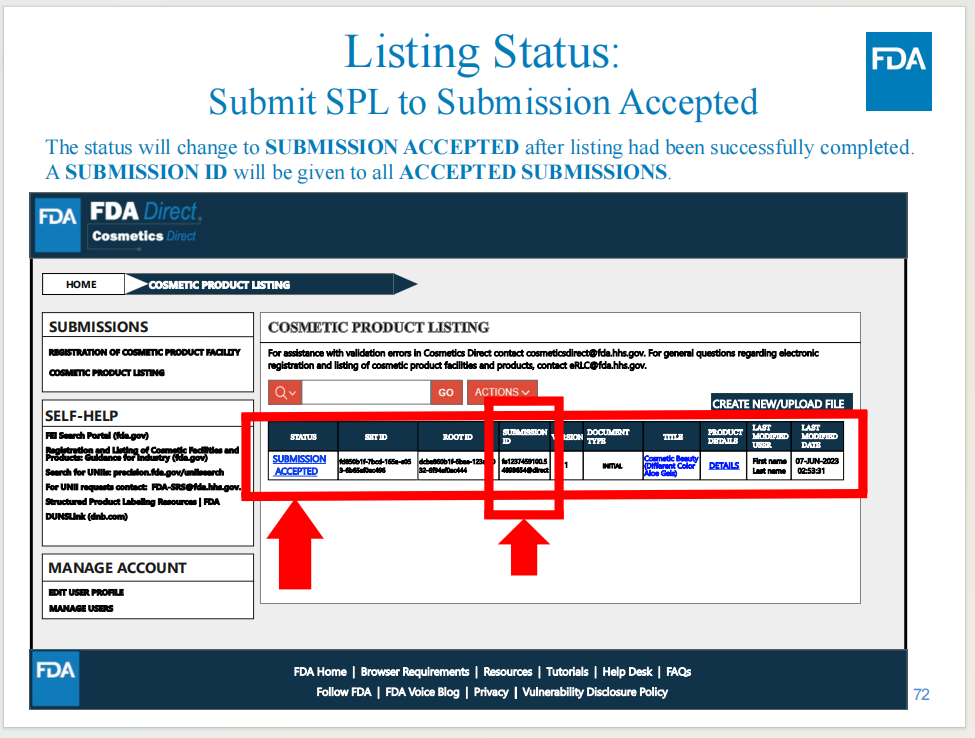
系统意见征询截至10月18日,妆研猜测系统正式上线的时间可能在10月底或11月初,距今年年底截止期12月29日已经非常接近。瑞欧提醒您,输美企业务必关注新系统的相关内容,可以提前为工厂注册和产品列名做准备,以免影响产品销售。
相关阅读:
美国MoCRA法规前沿 | 化妆品产品列名怎么做?需提交哪些信息?
美国MoCRA法规前沿 | 化妆品企业怎么做工厂注册?需提交哪些信息?
美国MoCRA法案细则发布,FDA对化妆品设施登记和产品列名指南征求意见
▼▼
关注“妆研24小时”
获取更多全球化妆品合规新资讯







 化学品合规
化学品合规
 化妆品合规
化妆品合规
 检验检测
检验检测
 安全管理智能化
安全管理智能化
 绿色低碳可持续
绿色低碳可持续
 药品合规
药品合规
 食品合规
食品合规
 食品接触材料/再生塑料
食品接触材料/再生塑料
 中国农药登记
中国农药登记
 境外农药登记
境外农药登记