近年农药行业面临着各种挑战,各大农药企业除深耕国内市场外也开始纷纷寻找新的市场机会,努力提升自身市场份额,将眼光不断投向国际市场。
欧盟一直以来都是农药登记的高端市场,欧盟严格的农药评审体系和高昂的费用也让很多企业望而却步。
相比较活性物质批准和制剂登记,欧盟原药等同性认定(Technical equivalence, TE)是进军欧盟市场较为快捷的通道之一。
原药产品一旦获得欧盟TE批准,企业可获得以下竞争优势:
是原药质量的品质保证,也是企业有力的品牌宣传;
一次批准,欧盟全境认可;
可掌握贸易自主权,自由选择贸易伙伴。
从2016年开始,瑞欧科技农化团队已经为60多家企业150多个原药产品完成了欧盟原药等同登记,逐渐形成规模效应,积累了欧盟原药等同登记项目数据库,也成功帮助企业获得了欧盟市场入场券。
那已经批准的物质都有哪些?都是在哪一阶段通过的?对将要申请等同的企业有哪些参考价值呢?我们对目前申请并已经获批的物质进行了总结分析,并分享给大家。
项目统计—活性物质种类
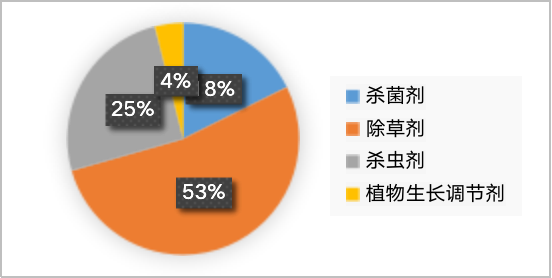
在获批的物质中,目前国内企业开展欧盟TE登记较多的原药产品类型涵盖杀虫剂、杀菌剂、除草剂、植物生长调节剂等(见下图),除草剂产品占据一半,杀虫剂和杀菌剂平分秋色,还有少量植物生长调节剂。这和欧盟农药的活性物质种类的数量比保持一致。
热门产品
除草剂 | 丙炔氟草胺,五氟磺草胺,烯草酮,唑啉草酯,烟嘧磺隆,异噁唑草酮,环磺酮等 |
杀菌剂 | 吡唑醚菌酯,丙硫菌唑,啶酰菌胺,氟啶胺等 |
杀虫剂 | 啶虫脒,氟啶虫酰胺,螺虫乙酯,康宽(氯虫苯甲酰胺)等 |
项目统计—评审阶段
欧盟原药等同登记的评审阶段分为两个,即Tier I(通常所说的“第一阶段”) 的化学组成评估,以及Tier II (通常所说的“第二阶段”)的毒理评估。项目在一阶段通过,还是在二阶段通过,会大大影响整个项目的成本和周期。
我们对获批的物质进行了分析(见下图),在瑞欧提交的TE项目中,60%以上的项目都在Tier I 就通过了,这主要归功于瑞欧对TE Tire I补资料的成熟应对,由此避免了部分项目进入第二阶段。对企业来说,Tire I能够通过自然是最好的,因为费用和周期都是最短的。
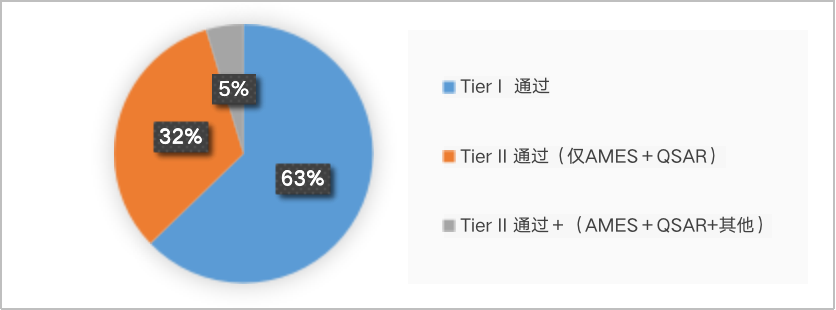
还有超过30%的项目,虽然是在Tier II 获得通过的,但是只是按照官方要求提交QSAR报告和Ames测试报告就获得通过了。这两份报告的周期比较短,费用也相对较低。
以上两种情况加起来占到所有TE项目的90%以上,也是最常见的情况。
还有剩下的不到10%的项目除了提交AMES和QSAR报告外,还提交了一些其他节点的数据,比如体外基因测试报告、皮肤致敏性实验数据等。这些额外报告一般是由于杂质的QSAR预测结果不理想导致。对于这些相对复杂项目,瑞欧也已经积累了一套成熟的解决方案体系,成功帮助企业用最少的成本满足欧盟TE评估的合规要求。
项目统计—常见问题
对于欧盟原药等同申请,合理有效的应对官方评审意见是帮助企业快速拿下欧盟TE批准信的关键,同时也可以帮助客户节省不必要的支出。
我们也总结了那些欧盟官方的常见评审意见,来看看你的产品是否会存在同样的问题呢?
五批次超过5年,或是3个月内的连续批次,如何说明样品代表性?
官方要求根据生产工艺推断是否可能产生SANCO 10597附件III中的相关杂质(如亚硝胺等)?
官方要求说明五批次检测方法下无法检出的杂质是否会残留在原药中?
官方要求补充理论上可能形成的杂质并进行说明?
如何说明杂质含量水平下风险可控?如何计算可接受的杂质限量范围?
针对这些常见问题,瑞欧科技已经准备了成熟的应对体系。针对物质的具体情况,为企业推荐合适的应对策略。
欧盟各个评估国在原药等同评估中遵循统一的法规和导则要求,同时在评审细节上的关注点又各有不同。随着欧盟评审负荷的加重,评审速度进一步放缓,熟悉评估国的评审风格,具备丰富的项目经验,是快速有效的推进TE等同项目的关键。
如果您对欧盟农药登记有任何问题,欢迎联系我们进行咨询交流,瑞欧科技将充分利用过去6年积累的丰富项目经验,为企业提供更具价值的专业法规服务。
「相关文章」








 化学品合规
化学品合规
 化妆品合规
化妆品合规
 检验检测
检验检测
 安全管理智能化
安全管理智能化
 绿色低碳可持续
绿色低碳可持续
 药品合规
药品合规
 食品合规
食品合规
 食品接触材料/再生塑料
食品接触材料/再生塑料
 中国农药登记
中国农药登记
 境外农药登记
境外农药登记