今年7月底,欧盟委员会发布了一项法规草案,提出消费者用途的危险混合物的毒物中心通报(PCN)延期一年实施,即从2020年1月1日推迟至2021年1月1日,并向公众征询意见。征询意见已于8月18日截止,目前显示大多数反馈都表示支持该项提议。毒物中心通报法规(Commission Regulation 2017/542)自2017年出台后在欧盟境内就颇受关注,随着原定截止期的临近,出口欧盟市场的企业也陆续收到欧盟境内进口商要求进行毒物中心通报。
9月2日,CRAC2019 化学品环境安全管理分会场上,来自英国国家化学品应急救援中心Giles Spencer Hobson先生分享了毒物中心通报实施进展,帮助出口危险混合物到欧盟市场的企业做好应对准备。

Giles Spencer Hobson先生
首先,毒物中心通报(PCN)是什么?
毒物中心通报,全称 Poison Center Notification(以下简称PCN)。
随着越来越多的化学产品(如清洁剂、油漆、粘合剂)投放到欧盟市场上,供公众日常生活和专业人员使用,意外接触或不当使用危险化学品的发生率也越来越高。每年欧盟毒物控制中心大概会接到600000个电话,在紧急情况下求寻医疗咨询和救助,特别是一些婴幼儿的意外接触,但是发生事件时大约40%的事件都遇到危险混合物成分识别问题,可能导致患者不必要的过度治疗或预防原因的住院。为此许多成员国建立了一个系统,从向市场投放危险混合物的企业收集信息。但是在先前的立法制度下,缺乏协调信息要求,企业在不同成员国的市场需要多次以不同格式提交类似信息。这种多样性也可能导致在不同成员国发生中毒或意外接触事件时,医务人员获得的信息不一致。
因此,2017年3月22日欧盟发布毒物中心通报法规(Commission Regulation 2017/542), 作为《关于物质和混合物的分类、标签和包装的法规》 (Regulation (EC) No 1272/2008) (简称CLP法规)的新附件VIII,来实施有关急救医疗响应时的协调信息要求。根据该法规,所有投放到欧盟市场并具有理化危险或健康危害的混合物,需要向成员国毒物中心提交通报,并引入了新要求—在危险混合物标签上附上唯一的配方标识符(UFI)。
PCN何时截止?
PCN的提交期限是基于危险混合物最终用途决定的,企业按照投放市场产品的最终用途需要在截止期限之前完成通报,具体的截止日期如下:
消费用途→2020年1月1日(计划延迟至2021年1月1日)
专业用途→2021年1月1日
工业用途→2024年1月1日
企业在通报过程中对混合物的最终用途的确认有一定难度,应尽量向下游用户收集用途信息,如果在提交后出现新的用途,则根据需要及时更新。
哪些产品可以不提交PCN?
PCN主要是针对投放欧盟市场的具有理化危险或健康危害的混合物,以下情况可豁免:
1. 单组分物质;
2. 不符合CLP要求的;
3. 仅有环境危害分类的;
4. 产品仅用于R&D和PPORDs;
5. 加压气体;
6. 爆炸物 (不稳定爆炸物和1.1项-1.6项的爆炸物) ;
以上豁免的产品也可以自愿通报。在自愿提交后,供应商可保护机密商业信息,也可有助于应急响应人员获取必要的信息以免过度治疗。
谁需要提交PCN?
PCN的提交人和责任主体是将危险混合物投放市场的欧盟境内进口商和下游用户(混合物配置商)。仅在市场上储存和放置混合物的分销商,在不进行任何其他混合物活动的情况下,原则上不需要向指定机构提交信息。但是,一些分销商对产品进行更换品牌、重新包装,或将产品投放到上游用户未通报的成员国市场,则仍需要向指定机构进行通报。
另外,PCN的责任主体可以委托第三方(比如代表子公司提交的母公司/总部、代表责任人的咨询机构)进行提交,但是不免除相应的责任。
PCN如何提交?
PCN旨在统一协调欧盟所有成员国的通报方式,其通报形式和具体内容如下:
• 统一使用毒物中心通报(PCN)格式提交
• 统一使用欧洲产品分类系统(EuPCS)给产品分类
• 统一使用ECHA建立的提交门户直接发送到混合物投放市场的成员国指定机构

• 统一的通报内容
基本信息 | 混合物危害信息 | 混合物成分信息 | 其他信息 |
产品标识 混合物成分标识(CAS/EC) 唯一的配方标识符(UFI) 提交人的联系信息 | 混合物分类 标签要素 毒理学信息 | 混合物的成分(100%) 混合物的成分浓度(精确浓度或范围) 成分的分类 | 包装类型、大小 颜色、状态、pH 产品类别(EuPCS) 用途(消费、专业、工业) |
PCN引入的新要求? —唯一的配方标识 (UFI)
唯一的配方标识(UFI)是由欧盟企业的增值税编号和分配给产品的内部代码生成的16位字母数字代码。一个UFI只能分配给一个混合物配方,同样的UFI可以在供应链中使用,只要成分不变。UFI可用来保护机密配方,作为已知的成分提交。
UFI可用软件自主生成,在提交时必须填写,通报审核通过后才“有效”,才能明确地将提交的混合物信息以及与患者治疗相关的信息与投放市场的特定产品联系起来。
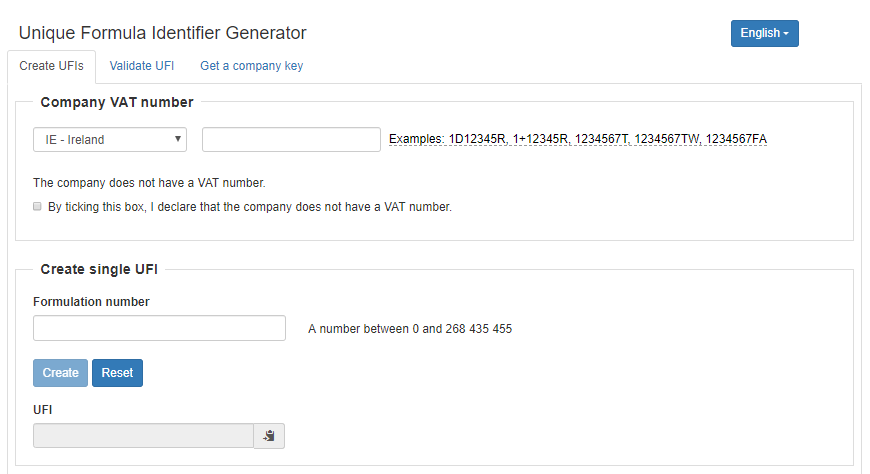
https://ufi.echa.europa.eu/#/create
UFI必须印在或贴在所有含有有害混合物的产品标签上。如果产品未贴标签(例如工业现场使用的某些产品或者无包装产品),UFI可在SDS中注明。

由此可见,欧盟市场上的绝大多数的混合物产品都要被管辖,且合规工作做起来并不简单,也因此促使欧盟委员会发布延期的征求意见稿。
征求稿中绝大多数的企业或协会的反馈意见都是建议延期,那么企业是否在通报中遇到了哪些困难呢?
后续,我们将推出PCN(下篇),关于UFI的显示、分配与管理等相关内容在后续专题中会继续科普。
如需了解更多欧盟PCN信息,可登陆毒物中心网站浏览更多资讯。







 化学品合规
化学品合规
 化妆品合规
化妆品合规
 检验检测
检验检测
 安全管理智能化
安全管理智能化
 绿色低碳可持续
绿色低碳可持续
 药品合规
药品合规
 食品合规
食品合规
 食品接触材料/再生塑料
食品接触材料/再生塑料
 中国农药登记
中国农药登记
 境外农药登记
境外农药登记