CRAC-HCF 2020的亚太地区法规专场已经圆满结束,相信各位来宾与观众都对亚太地区主要贸易国的化学品管理有了一定的了解。最值得关注的无疑是印度与越南即将在2021年出台全新的化学品法规。印度方面,在2021年的上半年预计出台一项对新化学物质与现有化学物质的统一管理法规,也就是Chemicals (Management and Safety) Rules,CMSR;而越南方面,则是要在Chemical Control Law下对新化学物质进行管理。在此对会议上关于印度与越南话题的重点内容进行更详细的总结与解读,以加深大家的理解。
印度CMSR草案最早发布于2019年11月,之后也历经多次公开与非公开的草案修订,最新一版的草案发布于2020年8月24日。该草案计划于2021年初实施,届时也将会对化学品行业产生不小的影响。
基于目前的CMSR草案内容,管控主要为两类物质:即新物质与现有物质。由于目前CMSR并没有建立现有物质名录,因此在法规实施一年后开启的预通报将会成为现有物质名录的基础,即在预通报期间内未获得通报证明的化学物质将被视为新物质。下表列出了对各位物质的合规要求:
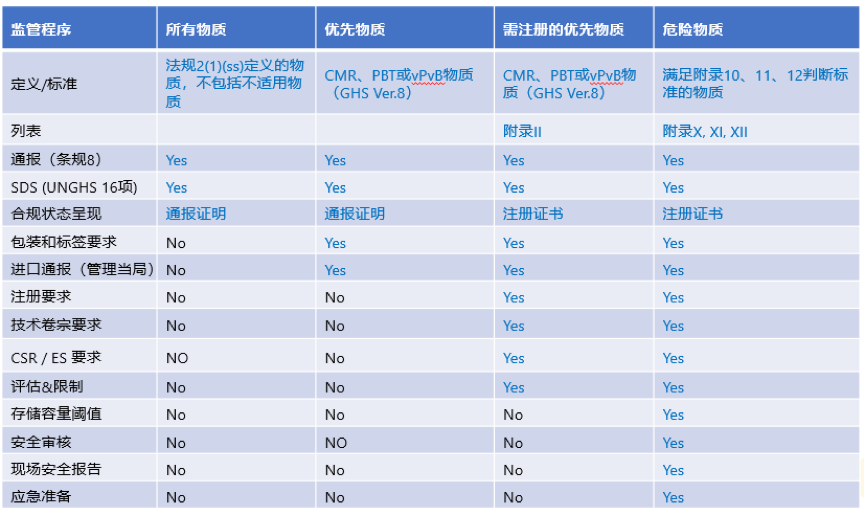
对于进出口活动而言,最需要关注的则是通报、注册及进口危化品所需的进口通报要求,从上表可以看出:现有物质与新物质均需要通报;附录2中列出的优先物质与附录10、11、12中的有害物质需要满足注册要求;而除此之外进口附录10、11、12的危险物质还需要进口通报。由于法规中对各类物质的要求与时间节点比较繁杂,在这里,我们将通报、注册、限制或禁止、危险物质监管的相关内容再次总结:
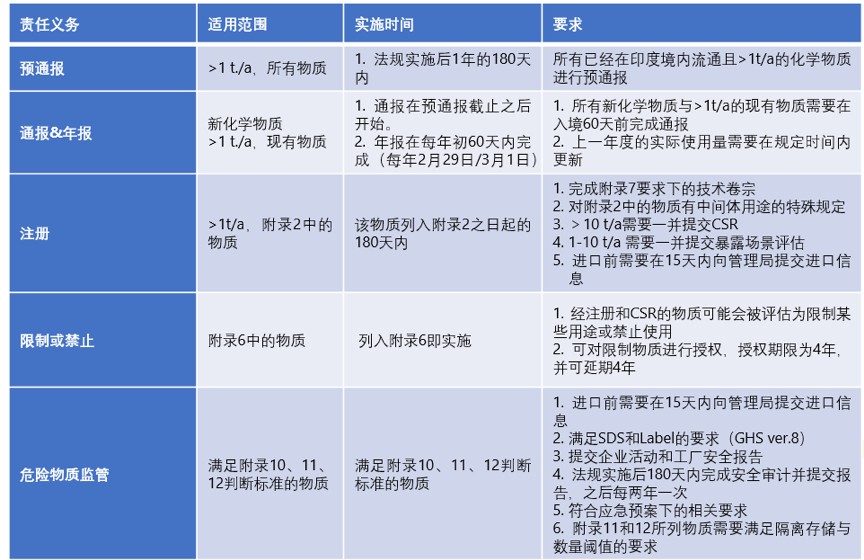
需要注意的是,草案规定在预通报截止期之后,所有未在该期间内通报的化学物质将被视为新化学物质。而新化学物质则需要在进口前60天内完成通报。需要准备的技术文件包括:
通报人信息(联系方式、外国生产商信息或国内生产信息)
基本的物质信息(名称、SMILES、组分信息、详细的结构信息)
分类(GHS ver.8)
用途
下游使用者
吨位量和最大存储量
需要注册的物质是首批附录2中的750个优先物质,当然在后期对通报物质的评估后也会相应加入更多需要注册的优先物质。注册则需要提交技术卷宗,其中也不乏详细的试验报告等。关于试验报告,印度优先采纳OECD GLP的试验报告,且相应的试验必须在印度NABL或GLP的实验室开展。在开展新试验前,也需要先向主管部门提交测试计划,而涉及到脊椎动物的体内试验则不到万不得已不优先考虑。
越南方面,最值得注意的就是今年来开放的两次国家名录增补窗口(National Chemical Inventory, NCI)。NCI将作为越南新物质法规的重要名录支撑。据目前统计截止到10月总共有41307个物质申请增补,而仅有8889个物质批准列入,大量的物质还处于缺少证据或信息不正确的状态。目前开放的NCI名录增补截止期为2021年4月15日,届时未列入名录中的将会被视为新化学物质。
关于NCI名录增补,需要由越南境内相关行业的企业在国家信息库平台上注册账号并完成资料提交,据了解,NCI名录增补对第三方咨询公司的要求较高,并非接收一般咨询公司的增补资料。所需要的资料有:
物质名称
产品SDS
流通于越南境内的证据(合同、invoice、清关证明等)
新化学物质法规的草案还在制定当中,据目前所了解,新物质法规将会对新化学物质划分为新化学物质和外国化学物质。外国化学物质则为被越南主管部门认可的外国化学品名录所列物质。新化学物质需要在进口或生产前取得相应的注册证,而相应的外国化学物质可能将会减免注册申报过程中的数据要求。
由于此次增补将会是越南NCI名录的最后一次增补,如果企业尚有产品流通越南,但未提交增补,也请抓住机会,以免在新物质法规实施后增加合规成本、影响正常的贸易。
以上是本次CRAC-HCF 2020亚太地区法规专场的总结,瑞欧也将持续关注印度与越南的法规进展,同时我们将提供全面的法规咨询服务:
1. 印度物质合规服务—通报、注册、年报
2. 印度物质测试服务—测试监理与评估报告撰写
3. 印度授权申请服务
4. 印度法规培训服务
5. 越南NCI名录增补服务
6. GHS服务
上述解读可通过点击下方链接观看直播回放









 化学品合规
化学品合规
 化妆品合规
化妆品合规
 检验检测
检验检测
 安全管理智能化
安全管理智能化
 绿色低碳可持续
绿色低碳可持续
 药品合规
药品合规
 食品合规
食品合规
 食品接触材料/再生塑料
食品接触材料/再生塑料
 中国农药登记
中国农药登记
 境外农药登记
境外农药登记