研发历程
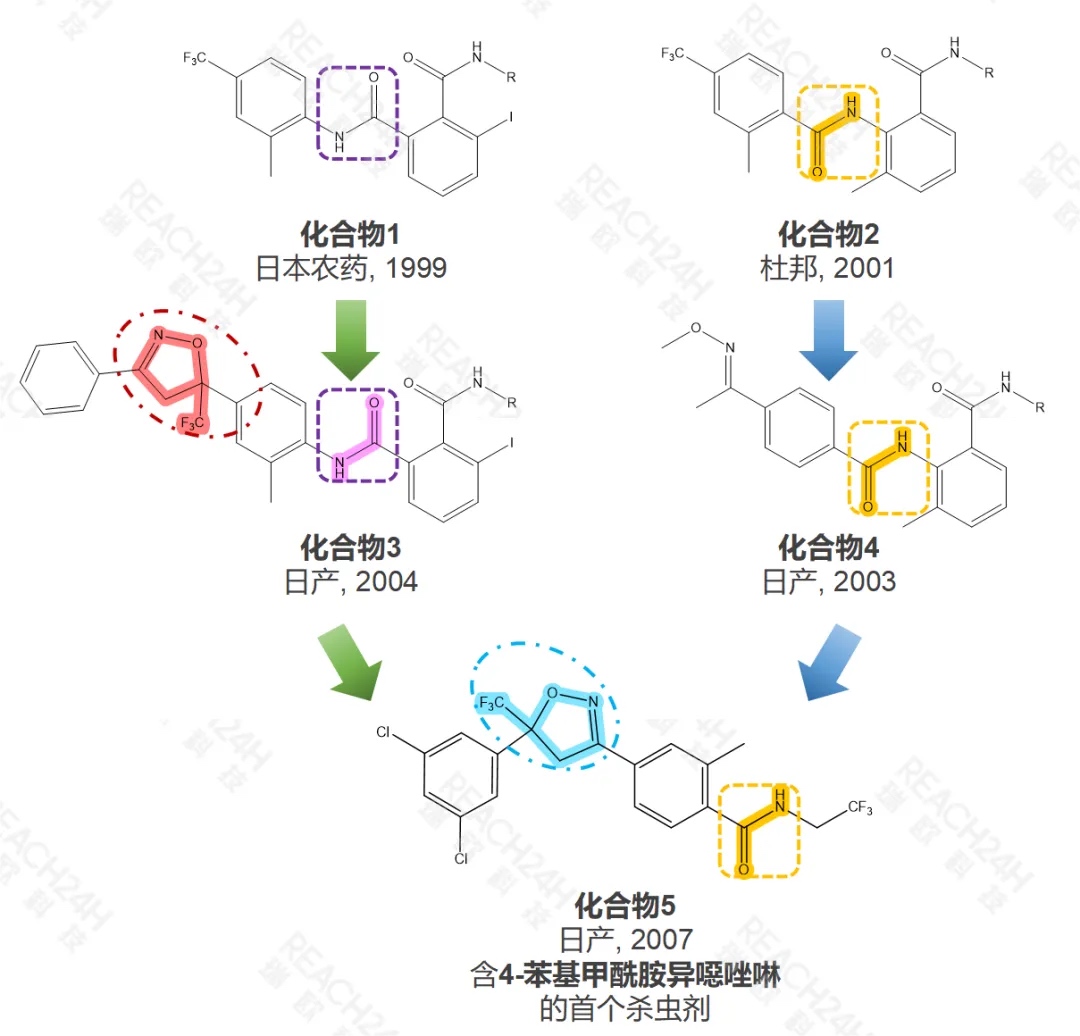
异噁唑啉类杀虫剂研发的开端可追溯至1999-2001年间,当时日本农药(Nihon Nohyaku)和杜邦(DuPont)分别发现了具有显著杀虫活性的邻苯二甲酰胺结构(化合物1)和邻氨基苯甲酸二甲胺结构(化合物2),且作用机制表明这两类结构的化合物都属于昆虫鱼尼丁受体(RyR)的选择性激活剂。
随后,日产(Nissan)分别对上述两类化合物进行结构优化。一方面,在2004年用含3-三氟甲基异噁唑啉基取代了化合物1中的三氟甲基,发现了首个具有潜在杀虫活性的含三氟甲基异噁唑啉结构(化合物3);另一方面,于2003年在化合物2的基础上引入了含肟的子结构,形成了新的邻氨基苯甲酸二甲胺结构(化合物4)。
日产又在2003-2004年间继续对化合物3和4开展进一步优化,并最终发现了首个含4-苯基甲酰胺异噁唑啉杀虫剂(化合物5),化合物5既继承了化合物3中的三氟甲基异噁唑啉结构,同时,它其中酰胺结构的方向又和化合物4中的保持一致。而更令人兴奋的是作用机制研究表明化合物5属于γ-氨基丁酸(GABA)门控氯离子通道变构调节剂,由此,一类含新颖分子骨架且具有独特作用机制的杀虫剂被正式宣布发现。
上市路径
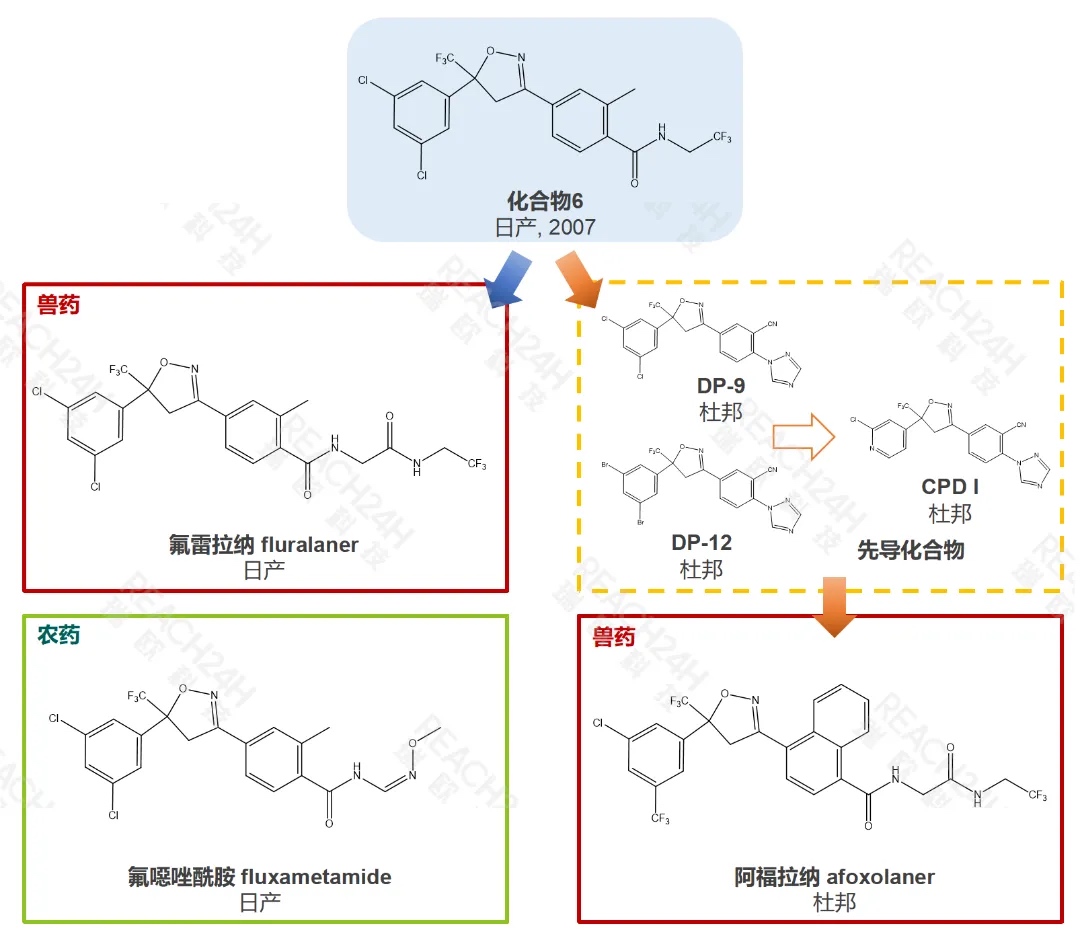
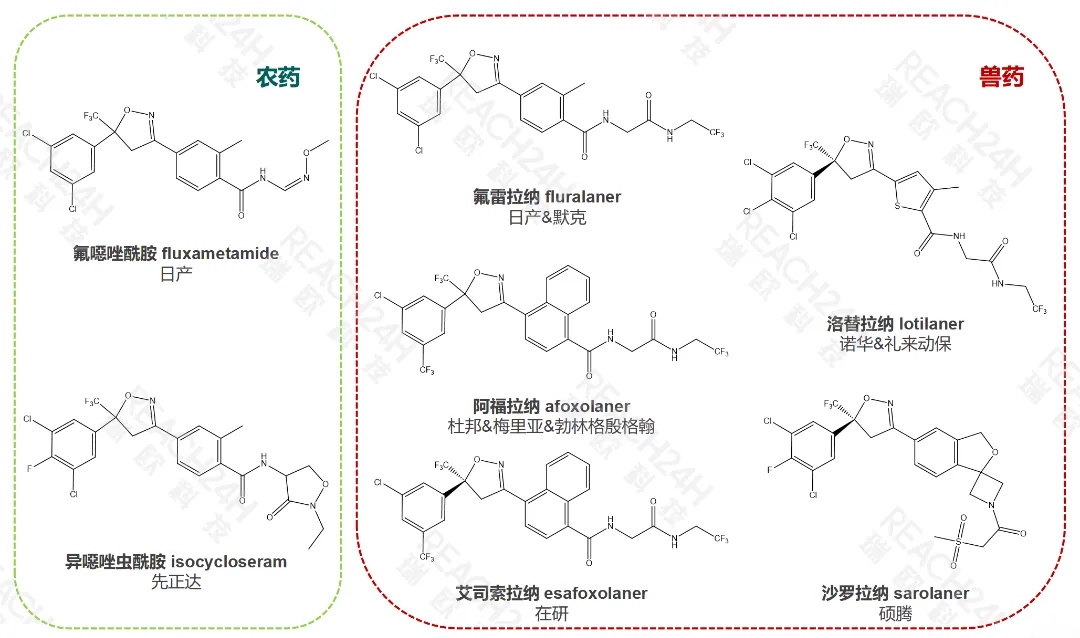
异噁唑啉类杀虫剂的商业化开发由日产和杜邦分别开启,日产首先开发了动物保健产品氟雷拉纳(fluralaner),用于治疗犬、猫体表的跳蚤或蜱感染。杜邦也紧随其后在先导化合物DP-9和DP-12的基础上开发了类似的动物保健产品的阿福拉纳(afoxolaner)。异噁唑啉类动物保健产品的成功上市,也是日产和杜邦与默克、梅丽亚、勃林格殷格翰等公司共同深入合作的成果。当前,异噁唑啉类动物保健产品的开发较为活跃,同类产品包括洛替拉纳(lotilaner)、沙罗拉纳(sarolaner)以及在研的艾司索拉纳(esafoxolaner)等。其中,洛替拉纳还进一步扩展到人用药领域,目前已被FDA批准用于蠕形螨睑缘炎的治疗。
在农用化学品方面,日产开发了首个异噁唑啉类杀虫剂氟噁唑酰胺(fluxametamide),该化合物早在2006年就已在日本、韩国、巴西、加拿大等国申请了专利,但直至2018年才在韩国率先上市,并于2019年也在日本上市,主要用于蔬菜、果树、棉花、茶树等作物,防治蓟马、粉虱、潜叶蝇、甲虫、红蜘蛛、锈螨等害虫和害螨。先正达的同类产品异噁唑虫酰胺(isocycloseram)商业化进展也较快,自2021年,异噁唑虫酰胺已经先后在阿根廷、韩国、澳大利亚、越南等国取得了登记批准。其他农化公司,如巴斯夫、住友、拜耳以及国内的清源农冠也正在积极布局相关产品。
作用机制阐明与类别
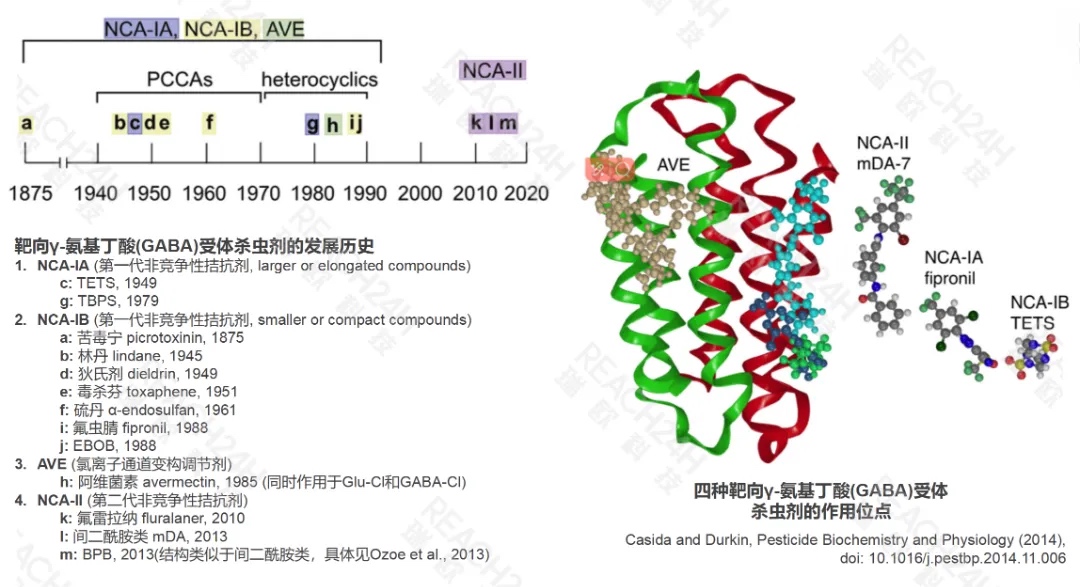
异噁唑啉类杀虫剂靶向的是昆虫体内的γ-氨基丁酸(GABA)受体,当前针对这一靶标蛋白的不同结合位点,已开发了4类不同作用机制的杀虫剂,且它们之间几乎不存在交互抗性。根据美国加州大学伯克利分校John E. Casida教授的分类,异噁唑啉类和间二酰胺杀虫剂同属于GABA受体的第二代非竞争性拮抗剂(NCA-II)。目前,IRAC已经将2种异噁唑啉类(氟噁唑酰胺和异噁唑虫酰胺)和1种间二酰胺类(溴虫氟苯双酰胺)归为第30组:γ-氨基丁酸(GABA)门控氯离子通道变构调节剂。
GABA是无脊椎动物中主要的抑制性神经递质,其受体由Rdl基因编码的亚基组成,并通常被称为Rdl GABA受体。脊椎动物的基因编码许多不同的亚基,可以形成大量复杂的异戊聚体,而功能性昆虫的GABA受体只能由Rdl亚基构成。因此,昆虫GABA受体在与脊椎动物在组成和药理学方面存在重要差异。尤其对于NCA-II来说,其结合位点在昆虫和哺乳动物之间具有明显的差异,因而具有选择性毒性。
中国科研团队的研发进展
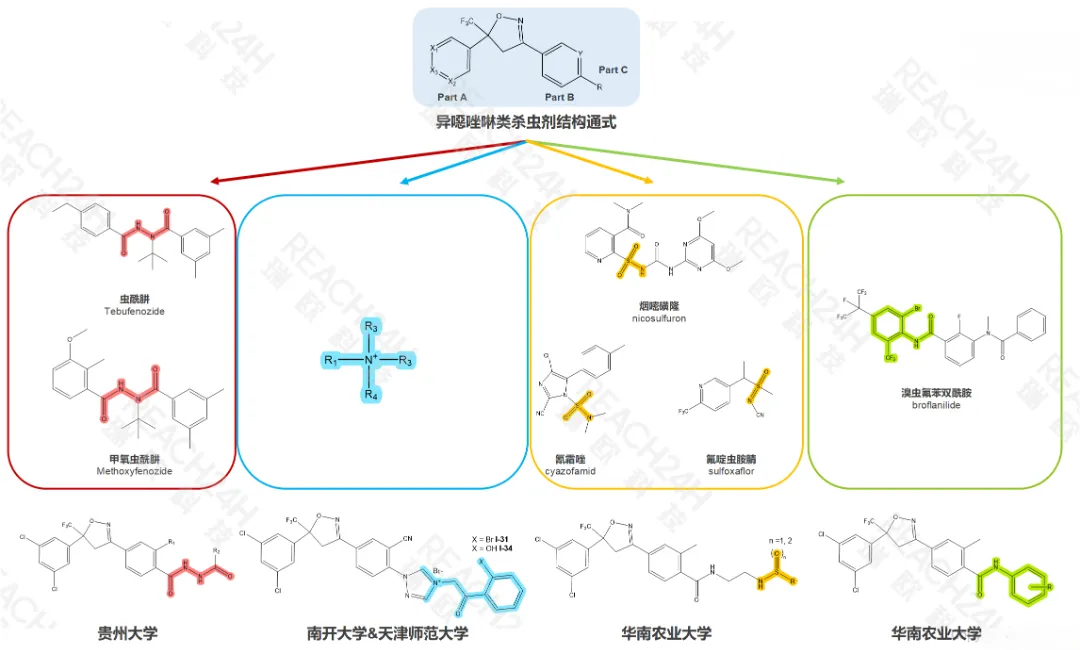
由于异噁唑啉类杀虫剂结构新颖且药效显著,贵州大学、南开大学、天津师范大学、华南农业大学等也紧跟前沿动态,并依托于“中间体衍生法”等理论基础,展开了技术攻关,研发了一系列新型异噁唑啉类杀虫剂。并且,对于氟雷拉纳蜜蜂毒性高毒的问题,也发现通过在分子骨架中引入磺酰胺或亚磺酰胺结构后能显著降低毒性。
同时,中国农科院和中科院动物所的科研团队也从分子层面揭示,氟噁唑酰胺中手性结构的活性和毒性具有对映体选择性,其中S-氟噁唑酰胺不仅活性更优,且对蜜蜂的毒性相比于消旋体显著降低。
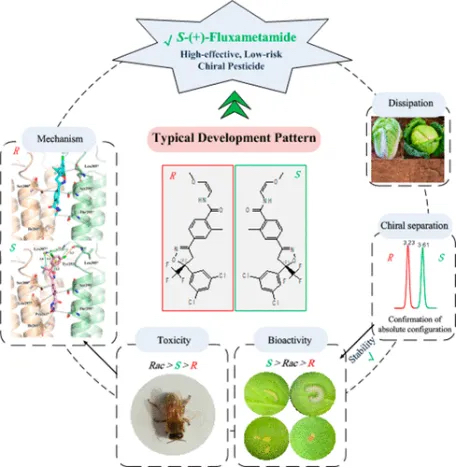
氟噁唑酰胺中手性结构的活性和毒性具有对映体选择性
Runan Li, et al. Environ. Sci. Technol. 2019, 53, 23, 13657–13665
农药登记难点剖析
与异噁唑啉类杀虫剂相比,IRAC同一组别下的溴虫氟苯双酰胺(间二酰胺类)已在中国、美国等更为重要的市场上市,并取得了极高的市场增长。但如上所述,异噁唑啉类杀虫剂目前仅在有限的国家取得登记批准,导致其农用市场并未完全打开。
对蜜蜂的影响是异噁唑啉类杀虫剂关注的重点,这一点对蜜蜂高毒的氟雷拉纳来说尤为重要。除此之外,异噁唑啉类杀虫剂对非靶标节肢动物和水生动物(特别是水生无脊椎动物)的影响也需要重点关注。在实际登记过程中,需要系统的进行风险评估并给出合理的风险降低措施,并根据风险评估的结果来有针对性的开展蜜蜂半田间或田间试验等高阶试验,以进一步明确相关产品的实际使用风险。
健康危害及风险也是当前全球新农药登记关注的重点,尤其是致突变、致畸和致癌的“三致作用”,一旦存在与人体相关的这些健康危害,根据中国、欧盟等国家和地区的农药登记政策将面临“一票否决”。对于异噁唑啉类杀虫剂来说,由于同时作为农药和兽药使用,较为充分的毒理学资料已表明这类杀虫剂不太可能具有致突变性和致畸性。但在兽药登记过程中通常可以减免致癌性相关的资料,所以当前异噁唑啉类杀虫剂的致癌性研究尚不充分。
根据先正达在澳大利亚农药登记已披露的信息,异噁唑虫酰胺不太可能具有致癌性。而根据日产在日本农药登记已披露的信息,氟噁唑酰胺在雄性大鼠中观察到甲状腺滤泡细胞腺瘤,并在雄性小鼠中观察到肝细胞腺瘤。虽然日本评审机构已排除了氟噁唑酰胺的遗传毒性致癌性,但相关非遗传毒性致癌性的人体相关性并未充分阐明。通常来说,啮齿动物中肝及甲状腺肿瘤的发生具有关联性,同时由PPARα激活等途径引起肝肿瘤也往往不具有人体相关性,因此针对氟噁唑酰胺在啮齿动物中观察的潜在致癌作用,仍需要进一步开展额外的作用机制研究以明确人体相关性。

农药风险评估步骤
启示与展望:农药的新质创新
从异噁唑啉类杀虫剂的研发到上市的整个过程来看,一方面,既需要基础研究的不断积累(如二甲酰胺结构的发现以及对GABA受体蛋白结构的解析),又需要幸运女神的眷顾(如三氟甲基异噁唑啉结构的创造性引入),因此整个新农药研发过程需要厚积薄发,且不断创新。可喜的是,我们也同时看到了中国科研团队正以理论为指导,紧跟前沿领域并持续攻关,必将终有回报。另一方面,异噁唑啉类杀虫剂上市的过程可谓一波三折,尤其是对农用化学品的登记批准来说。但正如诺奖得主詹姆斯·布莱克所说“一种药物如果没有被至少扼杀过三次,就不会是一种好药”,而这一说法同样适用于农药。唯有不断深入了解产品,充分明确安全性和适用场景,才能真正开发出一款成功的新农药产品。
参考文献
Asahi M, Kobayashi M, Kagami T, et al. Fluxametamide: A novel isoxazoline insecticide that acts via distinctive antagonism of insect ligand-gated chloride channels[J]. Pesticide biochemistry and physiology, 2018, 151: 67-72.
Blythe J, Earley F G P, Piekarska-Hack K, et al. The mode of action of isocycloseram: A novel isoxazoline insecticide[J]. Pesticide Biochemistry and Physiology, 2022, 187: 105217.
Casida J E, Durkin K A. Novel GABA receptor pesticide targets[J]. Pesticide biochemistry and physiology, 2015, 121: 22-30.
Gao Y C, Song X, Jia T, et al. Discovery of new N-Phenylamide Isoxazoline derivatives with high insecticidal activity and reduced honeybee toxicity[J]. Pesticide Biochemistry and Physiology, 2024: 105843.
Huang S, Zhu B, Wang K, et al. Design, synthesis, and insecticidal and fungicidal activities of quaternary ammonium salt derivatives of a triazolyphenyl isoxazoline insecticide[J]. Pest Management Science, 2022, 78(5): 2011-2021.
Lahm G P, Cordova D, Barry J D, et al. 4-Azolylphenyl isoxazoline insecticides acting at the GABA gated chloride channel[J]. Bioorganic & medicinal chemistry letters, 2013, 23(10): 3001-3006.
Li R, Pan X, Wang Q, et al. Development of S-fluxametamide for bioactivity improvement and risk reduction: systemic evaluation of the novel insecticide fluxametamide at the enantiomeric level[J]. Environmental science & technology, 2019, 53(23): 13657-13665.
Liu C, Guan A, Yang J, et al. Efficient approach to discover novel agrochemical candidates: intermediate derivatization method[J]. Journal of agricultural and food chemistry, 2016, 64(1): 45-51.
Li Y, Zhang W, Wu Z, et al. Design, synthesis, and insecticidal activity of novel isoxazoline diacylhydrazine compounds as GABA receptor inhibitors[J]. Journal of Agricultural and Food Chemistry, 2023, 71(17): 6561-6569.
Ozoe Y, Asahi M, Ozoe F, et al. The antiparasitic isoxazoline A1443 is a potent blocker of insect ligand-gated chloride channels[J]. Biochemical and biophysical research communications, 2010, 391(1): 744-749.
Ozoe Y, Kita T, Ozoe F, et al. Insecticidal 3-benzamido-N-phenylbenzamides specifically bind with high affinity to a novel allosteric site in housefly GABA receptors[J]. Pesticide biochemistry and physiology, 2013, 107(3): 285-292.
Shoop W L, Hartline E J, Gould B R, et al. Discovery and mode of action of afoxolaner, a new isoxazoline parasiticide for dogs[J]. Veterinary Parasitology, 2014, 201(3-4): 179-189.
Yang S, Tang J, Li B, et al. Rational design of insecticidal isoxazolines containing sulfonamide or sulfinamide structure as antagonists of GABA receptors with reduced toxicities to honeybee and zebrafish[J]. Journal of Agricultural and Food Chemistry, 2023, 71(39): 14211-14220.
相关阅读:










 化学品合规
化学品合规
 化妆品合规
化妆品合规
 检验检测
检验检测
 安全管理智能化
安全管理智能化
 绿色低碳可持续
绿色低碳可持续
 药品合规
药品合规
 食品合规
食品合规
 食品接触材料/再生塑料
食品接触材料/再生塑料
 中国农药登记
中国农药登记
 境外农药登记
境外农药登记