法规概述
药包材的定义和分类
《中国药典》中规定药包材是指药品生产企业生产的药品和医疗机构配制的制剂所使用的直接接触药品的包装材料和容器。此外,不直接接触药品但是对药品产生作用的药品包材(例如,不直接接触药品的铝塑包装,具有隔氧隔水的作用),也需要作为药包材进行登记监管。
对药包材通常分为高风险和非高风险两类,其中高风险药包材一般包括:
用于吸入制剂、注射剂、眼用制剂的药包材;
国家药品监督管理局根据监测数据特别要求监管的药包材;
中国药包材监管标准及模式
《中国药典》作为国家药品标准体系的重要组成部分,连同颁布的《中华人民共和国药品管理法》,《中华人民共和国药品管理法实施条例》,《药包材登记资料要求》以及各类技术指导原则通告为指导,加上国家药包材标准(简称YBB标准)共同组成了药包材监管的法规体系。根据国家药品监督管理局公告(2019年第56号公告)内容,中国对药包材的监管由以往的注册管理制度变为登记制度,并与药品制剂或原料药进行关联技术审评,使得审批审评更为高效和科学。

中国对药包材的监管
监管部门及其职责
![]()
国家药品监督管理局(NMPA)隶属于国家市场监督管理总局,该机构主要负责:
根据各省监督检查开展的情况和需要,适时修订相关检查标准;
根据需要组织对原料药、药用辅料和药包材开展现场检查和检验。
![]()
药品审评中心(CDE)隶属于NMPA,该机构主要负责:
建立原料药、药用辅料和药包材的登记平台与数据库;
原料药、药用辅料和药包材登记资料的接收、完整性审查、登记号授予和公示以及原料药、药用辅料和药包材与药品制剂关联审评审批。
![]()
省级药品监督管理局隶属于NMPA,对当地的药包材厂商施行监管。各省局主要职责包括:
对本行政区域内的原料药、药用辅料和药包材生产企业的日常进行监督管理;
根据登记信息对药包材供应商加强监督检查,依法依规及时查处存在质量问题的产品,并对已上市产品开展评估和处置;
登记流程
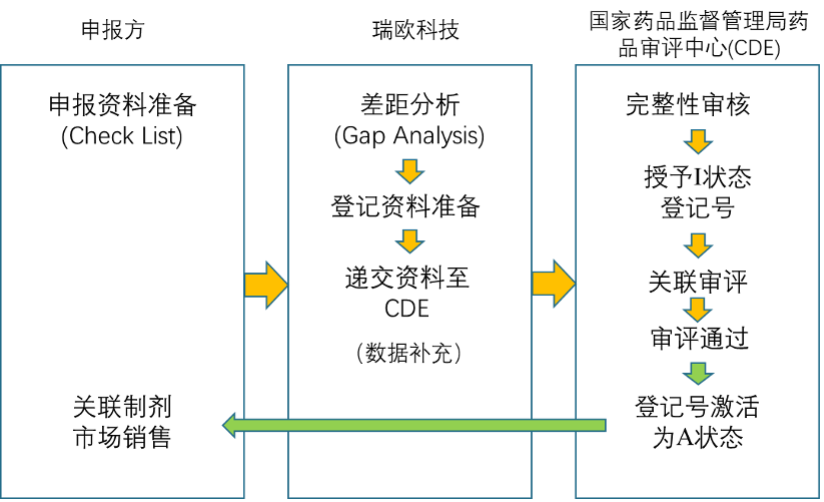
药包材登记流程图
药包材登记步骤
在CDE门户网站填写药包材的基本信息,并将登记资料以光盘形式提交至CDE;
CDE在收到资料后5个工作日内,对登记资料进行完整性审查;
当资料不齐全时,需要药包材企业对登记资料进行补充直至符合要求。CDE会对相关登记信息进行公示,并授予I状态登记号(登记号组成:B+四位年号+七位流水号);
当药包材通过关联审评后,登记号激活为A状态。
药包材登记资料
《国家药监局关于进一步完善药品关联审评审批和监管工作有关事宜的公告(2019年 第56号)》根据使用情况对药包材的分为以下类别:
未在境内外上市药品中使用过的药包材(如新材料、新结构);
已在境内外上市药品中使用过,但改变药品给药途径且风险提高的药包材;
未在境内外上市药品中使用过,但是可证明在食品包装中使用过的与食品直接接触的药包材(仅限用于口服制剂);
已在相同给药途径的上市药品中使用过的药包材;
其他
根据使用情况或所接触药品的风险不同,所提供的登记资料要求不同。大致包括内容如下:
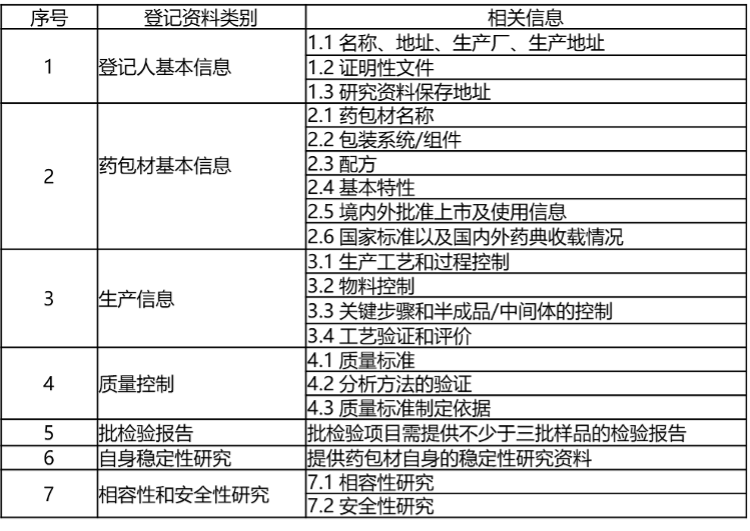
备注:采用相同的生产工艺和材料、具有相同功能的产品可以作为同一药包材登记,药包材企业可在同一个登记号下对其生产不同的型号和规格进行登记。
我们的服务
药包材登记咨询
药包材登记业务代理
登记备案资料翻译
药包材关联评审跟进
药包材年度报告
实验室委托及测试监理
官方问询沟通
我们的优势
超过13年法规研究和包材注册申报工作经验;
曾经成功申报的药包材包括:玻璃输液瓶、塑料输液瓶、粉液双室袋、液液多室袋、组合盖、胶塞、异戊二烯垫片、预灌封注射器、注射剂西林瓶、口服液体塑料瓶、口服固体塑料瓶、口服固体复合膜、塑料安瓿、玻璃安瓿等等。






 化学品
化学品
 食品接触材料
食品接触材料
 化妆品
化妆品
 绿色双碳
绿色双碳
 境外农药登记
境外农药登记
 中国农药登记
中国农药登记